



 有临
有临
 Feb 06,2020
Feb 06,2020
 3217
3217
在2020年春节这个特殊的节日里,关于新型冠状病毒(2019-nCOV)疫情的报道时刻牵动着我们的心。截至2月6日11时,全国确诊病例共计28060例,疑似病例共计24702例,从疫情趋势来看,这场抗击疫情的保卫战似乎还处在非常激烈的状态。在这个困难的时刻,从最前线的白衣天使,到最后方的物资供应,都出现了很多可爱可敬的战“疫”英雄。在这些每天实时更新的数字背后,是很多承担病毒核酸检测工作的实验人员的辛勤付出。他们的工作对于患者的临床诊断、治疗监测和隔离接触都至关重要,可以说是守卫着抗击疫情的“第二战场”。小编作为一名从事实验室检测工作的研发人员也为他们骄傲和自豪。

关于病毒核酸检测实验室
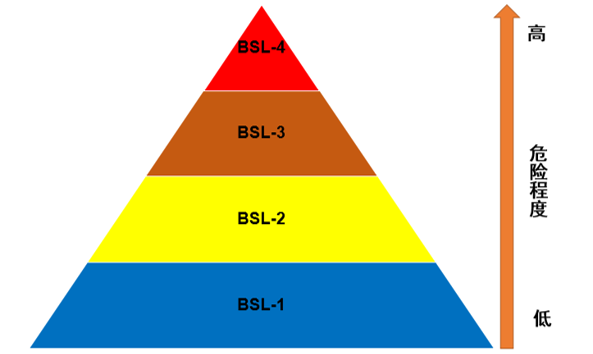
对于疑似病例的快速确诊,需要足够多的医务人员,符合检测条件的实验室,还要有足够的实验仪器和材料。即使人员和仪器材料都到位了,也并不是所有的实验室都可以承担检测工作。根据目前掌握的新型冠状病毒的生物学特点、流行病学特征、临床资料等信息,该病原体暂按照病原微生物危害程度分类中第二类病原微生物进行管理。根据国家卫健委发布的防控方案,新型冠状病毒的检测必须在符合生物安全要求的实验室由经过相关技术安全培训的人员进行操作。对于未经培养的感染性材料,在采用可靠的方法灭活前进行的病毒抗原检测、血清学检测、核酸提取、生化分析,以及临床样本的灭活等操作应当在生物安全二级实验室进行,同时采用生物安全三级实验室的个人防护。
关于标本
根据国家卫健委发布的《新型冠状病毒感染的肺炎实验室检测技术指南(第三版)》(下称“技术指南”),标本采集人员应经过生物安全培训合格并具备相应的实验技能,个人防护装备要求N95及以上防护口罩、护目镜、连体防护服、双层乳胶手套、防水靴套;如果接触了患者血液、体液、分泌物或排泄物,应及时更换外层乳胶手套。
标本种类包括上呼吸道标本(咽拭子、鼻拭子、鼻咽抽取物等),下呼吸道标本(深咳痰液、呼吸道抽取物、支气管灌洗液、肺泡灌洗液、肺组织活检标本),血液/血清标本,眼结膜标本,便标本。每个病例必须采集急性期呼吸道标本(包括上呼吸道标本和下呼吸道标本);重症病例优先采集下呼吸道标本(如支气管或肺泡灌洗液等);出现眼部感染症状的病例,需采集眼结膜拭子标本;出现腹泻症状的病例,需留取便标本。
标本采集后在生物安全二级实验室生物安全柜内分装。所有标本应放在大小适合的带螺旋盖内有垫圈、耐冷冻的样本采集管里,拧紧。容器外注明样本编号、种类、姓名及采样日期。密闭后的标本放入大小合适的塑料袋内密封,样本包装要求要符合《危险品航空安全运输技术细则》相应的标准。涉及外部标本运输的,应根据标本类型,按照A类或B类感染性物质进行三层包装。
用于病毒分离和核酸检测的标本应尽快进行检测,能在24小时内检测的标本可置于4℃保存;24小时内无法检测的标本则应置于-70℃或以下保存(如无-70℃保存条件,则于-20℃冰箱暂存)。血清可在4℃存放3天,-20℃以下可长期保存。应设立专库或专柜单独保存标本。标本运送期间应避免反复冻融。
关于病毒核酸检测流程
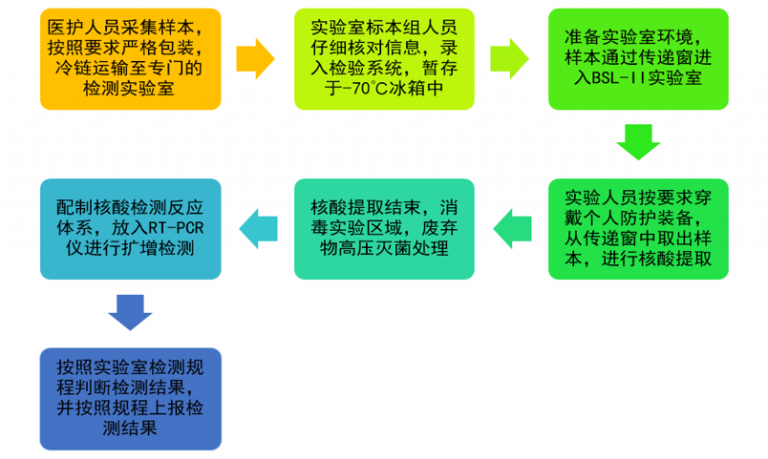
新型冠状病毒感染的常规检测方法是通过实时荧光RT-PCR 鉴定。目前的检测方法主要针对新型冠状病毒基因组中开放读码框1ab(open reading frame 1ab, ORF1ab)和核壳蛋白(nucleocapsid protein,N)。具体的检测流程包括标本采集、核酸提取、实时荧光RT-PCR扩增检测等。每做一批检测,从样本接收登记、实验环境准备、个人防护装备、实验检测及废弃物无害化处理,整个过程约6个小时。很多实验人员一天进行两批次检测,意味着每人需要全副武装、不间断地工作12小时。因为手部长时间捂在橡胶手套里,汗水无法排除,很多人手上长满了红斑。但是他们没有退缩,因为有那么多人等着结果。向他们致敬!
关于病毒核酸检测结果
阴性:无Ct值或Ct≥40。阳性:Ct值<37,可报告为阳性。
灰度区:Ct值在37-40之间,建议重复实验,若重做结果Ct值<40,扩增曲线有明显起峰,该样本判断为阳性,否则为阴性。如果用的是商品化试剂盒,则以厂家提供的说明书为准。
在实验室要确认一个病例为阳性,满足以下条件:同一份标本中新型冠状病毒2个靶标(ORF1ab、N)特异性实时荧光RT-PCR检测结果均为阳性。如果出现单个靶标阳性的 检测结果,则需要重新采样,重新检测。
需要指出的是,阴性结果也不能排除新型冠状病毒感染,需要排除可能产生假阴性的因素,包括:样本质量差,比如口咽等部位的呼吸道样本;样本收集的过早或过晚;没有正确的保存、运输和处理样本;技术本身存在的原因,如病毒变异、PCR抑制等。
关于病毒核酸检测试剂盒
截至2月6日,国家药监局共应急审批通过6家企业7个核酸检测试剂盒。其中6个试剂盒采用荧光PCR法,1个采用联合探针锚定聚合测序法。这些产品均为新型冠状病毒(2019-nCoV)感染的肺炎的辅助诊断及应急储备,在诊断的灵敏度、特异性和准确性等方面还有待更多临床应用数据的支持。值得注意的是,病毒核酸检测试剂盒由于研发时间紧,生产流程复杂,质量参差不齐,存在诸多方面的局限性:比如核酸检测稳定可靠性尚存疑;核酸检出率低,许多病例要重复2-3次检测;很多病人咽拭子阴性但肺细胞灌洗液里有病毒;目前等待核酸检测人数大大超过检测能力,仓促上阵得出的检测结果可靠性不高;漏诊、错诊等现象已经引起越来越多的关注。因此,有专家表示,对新型肺炎的诊断不应仅仅依赖于分子检测,按照传染病防治“宁错勿漏”的原则,建议依据CT病变范围结合临床资料,如血氧饱和度判断患者轻重缓急,重症优先住院,轻者尽快隔离。

此外,面对日益增加的疑似病例,即便有了检测试剂盒,检测时间也相对快速,检测资源仍旧是供不应求。因此,各大IVD企业正在全力研发更快速、更简便的快检试剂。截至2月6日,已报道三家IVD企业研发出新型冠状病毒快检试剂,均通过胶体金免疫层析法的技术进行检测。虽然快速检测的可靠性尚且存疑,小编还是希望这类试剂盒能够尽快投产,应用于广大基层医疗机构的早期筛查和诊断,不仅有助于加快诊疗,也利于防止大型医院密集检查而导致的交叉感染。
近期,面临大面积返程和复工,湖北外城市的本地散发病例随着复工和复学可能产生新的二代病例,存在大规模传播的风险,应注意加强防范,建议有条件的企业可以通过快速核酸检测排查隐患。相关临床试验入组要按各中心要求暂缓,在疫情没有解除之前确要入组的需要格外谨慎,入组筛查和清洗期后每周期入组前均建议进行新冠排查,随访和监察以远程为宜。
*图片或引用如有侵权,请联系删除