



 有临
有临
 2023.12.28
2023.12.28
 2915
2915
CDK4/6抑制剂介绍
细胞周期依赖性蛋白激酶(CDKs)是细胞周期调控机制的核心部分,也是多种恶性肿瘤的开始和进展所必需的。CDK4/6抑制剂通过靶向抑制cyclinD-CDK4/6复合物的活性,抑制Rb蛋白磷酸化与E2F转录因子释放,继而阻滞细胞周期从G1期进入S期,最终抑制肿瘤细胞增殖。
目前,CDK4/6抑制剂主要联合内分泌治疗,因雌激素受体(ER)与cyclinD-CDK4/6复合物存在多重交互作用[1]:(1)cyclin D是ER直接靶基因;(2)ER可诱导E2F活化启动非雌激素依赖性转录级联,促进肿瘤细胞增殖;(3)cyclin D可以直接结合ER,继而通过非CDK依赖性途径促进ER靶基因表达。
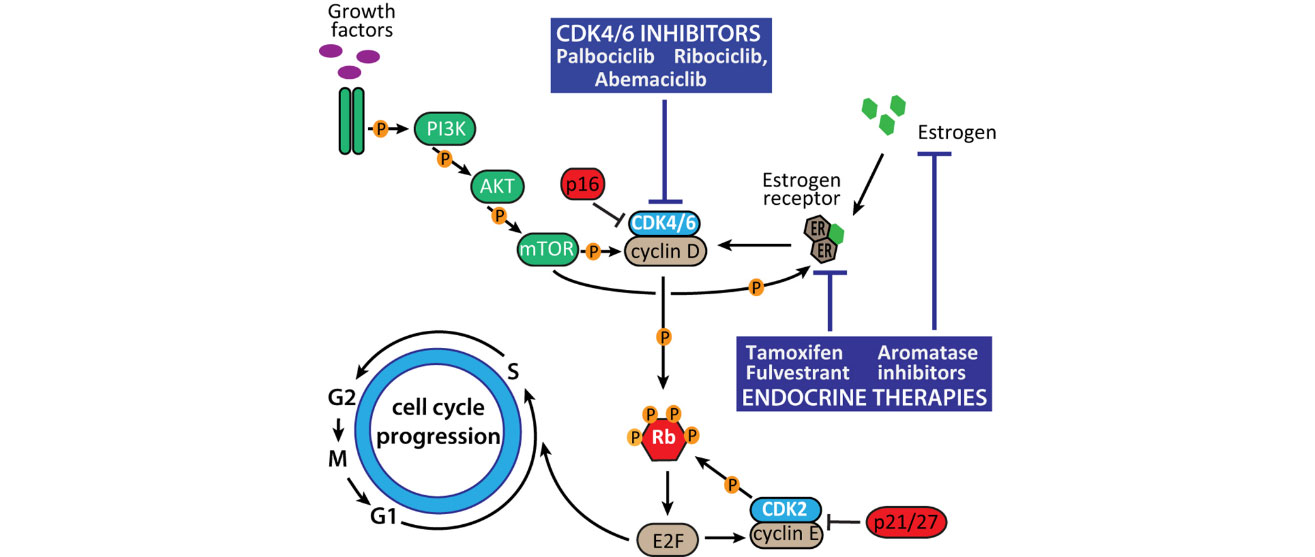
图1 CDK4/6抑制剂对细胞周期的作用机制
机遇一一临床未被满足的需求和临床推荐地位
根据世界卫生组织公布的2020年最新癌症数据[2],乳腺癌的新发病例数(226万)已经超过肺癌(220万),成为全球最高发的癌症。我国乳腺癌发病率增速较世界平均水平更高,发病高峰年龄为45岁至50岁。据中国癌症中心报告,2020年中国新发乳腺癌42万例,且年轻化趋势明显,整体而言较美国年轻约10岁。乳腺癌中HR+/HER2-乳腺癌是占比最高的亚型,约占所有乳腺癌的70%[3]。晚期乳腺癌的形势更为严峻,其带来的巨大疾病负担和社会负担。
对于HR+/HER2-晚期乳腺癌,CDK4 /6 抑制剂联合芳香化酶抑制剂或氟维司群一线或二线及以上治疗均可大幅度降低疾病进展或死亡风险,CDK4/6抑制剂联合内分泌治疗方案已成为临床治疗HR+/HER2-晚期乳腺癌患者的标准方案,奠定了CDK4/6在晚期一线或后线地位。CDK4/6抑制剂未来的研究方向是从早期到晚期,从新辅助/辅助到晚期治疗进展后选择的多元化。此外,CDK4/6抑制剂本身除了作用于细胞周期之外,还有免疫调节的作用机制,联合免疫治疗也是未来非常重要研发方向之一。
挑战一一竞争激烈与耐药
目前国内共有5款CDK4/6抑制剂上市,其中用于乳腺癌的有4款,分别是哌柏西利、阿贝西利、达尔西利和瑞波西利。虽然这4款药品在国内获批的适应症对象都是HR+/HER2-的晚期乳腺癌患者,但在适应症数量和使用范围上存在差异(见下表)。除此之外,阿贝西利也可以联合内分泌治疗用于HR+/HER2-、淋巴结阳性,高复发风险的早期乳腺癌成人患者的辅助治疗,也是目前国内唯一被批准用于早期乳腺癌患者的CDK4/6抑制剂。2023年,国内还有毗罗西尼和来罗西利申请上市审批。
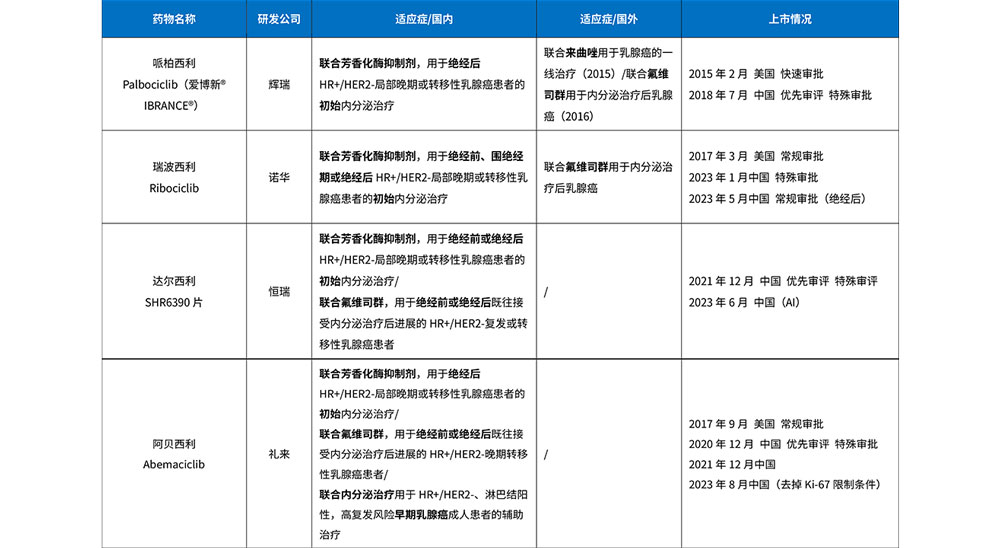
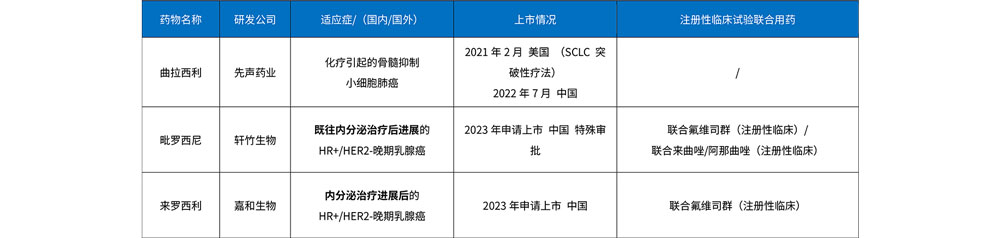
虽然CDK4 /6抑制剂联合内分泌治疗已奠定了晚期乳腺癌一线及二线的标准治疗地位,但对特定人群以及不同的CDK4 /6抑制剂间的临床差异未有明确结论。并且随着越来越多的患者使用CDK4/6抑制剂和内分泌作为一线标准治疗,不可避免地需要面对CDK4/6抑制剂进展之后的治疗方案选择。患者耐药机制复杂多样,主要包括细胞周期特异性机制及细胞周期非特异性机制。目前仍缺乏标准推荐,需结合既往治疗情况、疾病进展情况、既往治疗获益具体情况等进行个体化治疗方案选择。CDK4/6抑制剂无交叉耐药现象,但在疾病进展后是否可以跨线继续使用,仍在进一步探索。小样本研究显示派柏西利在CDK4/6抑制剂后线治疗的应用未有明显获益。但瑞波西利的MAINTAIN研究显示CDK4/6治疗进展后,瑞波西利联合氟维司群/依西美坦依然可显著改善PFS。基于此,2023年CSCO指南中将另一种CDK4/6抑制剂跨线治疗作为2A级别推荐。针对CDK4/6抑制剂耐药,多种基因表达的分子评价未能检测到一个疗效预测的准确标志物。表明CDK4/6抑制剂耐药问题不是某个单一的机制所致,是多种机制互相作用的结果。不同患者可能耐药机制都不一样,可能需要根据不同的生物标志物来判断个体的耐药原因,从而决定CDK4/6抑制剂治疗失败后应对策略。更多的联合治疗策略也在不断探索,未来还应建立于生物标志物指导下的精准治疗策略,以及不同治疗的最佳使用顺序等。
参考文献:
[1] Global CDK4/6 Inhibitors for Breast Cancer Market Briefing 2020, Trends, Applica.
[2] Siegel RL, Miller KD, Fuchs HE, et al. Cancer statistics, 2022. CA Cancer J Clin. 2022 Jan;72(1):7-33.
[3] Hart, C.D., Migliaccio, I., Malorni, L., et al. Challenges in the Management of Advanced, ER-Positive, HER2-Negative Breast Cancer. Nature Reviews Clinical Oncology, 2015:12, 541-552.