



 有临
有临
 2024.10.30
2024.10.30
 739
739

复发难治性结外NK/T细胞淋巴瘤(R/R ENKTL)是一种罕见的侵袭性非霍奇金淋巴瘤,晚期和复发或难治性ENKTL的5年生存率往往不足30%。在中国获批用于治疗R/R外周T细胞淋巴瘤(包括ENKTL)的靶向治疗药物西达本胺的ORR为18.8%,完全缓解(CR)率为6.3%(Shi et al, Ann Oncol 2015)。中山大学肿瘤防治中心黄慧强教授团队进行了GEMSTONE-201研究(迄今为止报告的评估抗PD-L1单抗治疗R/R ENKTL的最大注册研究),评估了suge治疗R/R ENKTL的疗效和安全性。研究结果近日发表于《Signal Transduction and Targeted Therapy》。
01. 研究方法-影像评估相关
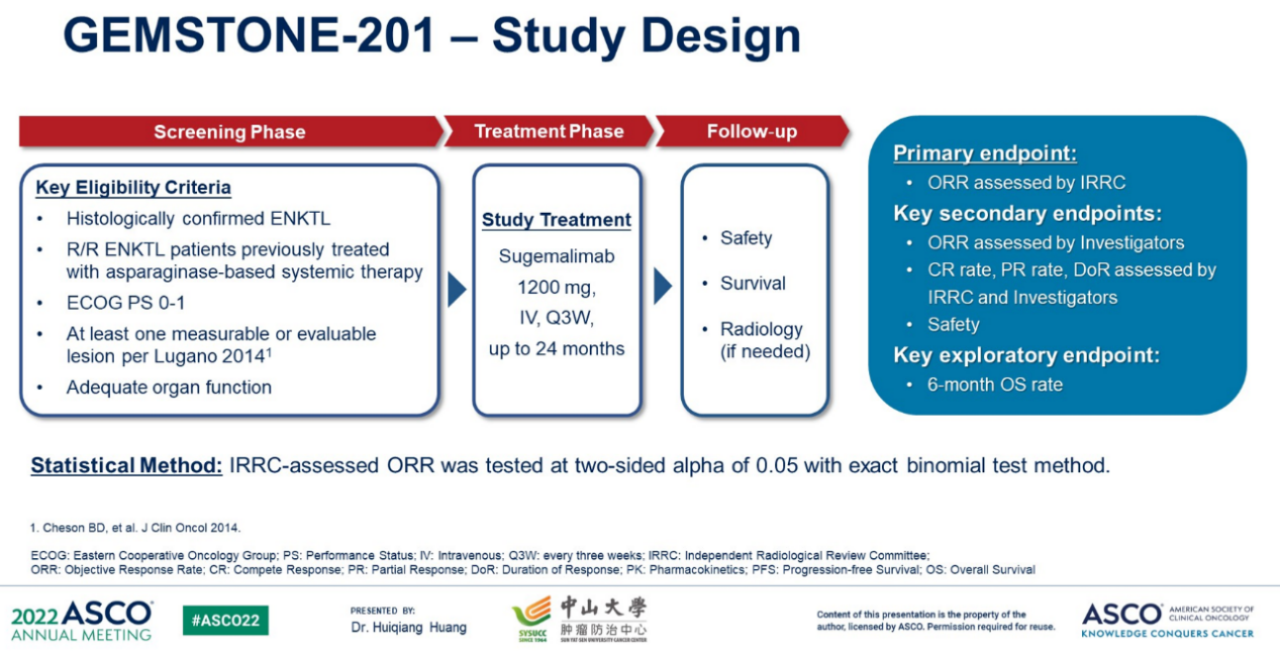
主要终点是独立影像评估委员会(IRC)根据Lugano 2014标准评估的总缓解率(ORR)(CR率+PR率)。关键次要终点包括研究者评估的ORR、CR率、PR率、IRC和研究者评估的缓解持续时间(DOR)以及安全性。

02. 影像疗效评估标准-Lugano2014
Lugano是关于霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL)的初始评估、分期以及治疗反应评估的指南。淋巴瘤治疗的疗效评估分为影像学缓解(CT/MRI 评效)和代谢缓解(PET/CT 评效),将FDG-PET与CT/MRI结合使用,作为FDG亲和性淋巴瘤的标准分期工具。使用5PS评分系统评估FDG亲和性组织学的治疗反应。
(1)CT/MRI评估
在CT上标记6个最大的靶病灶:
l 可以是淋巴结,淋巴结肿块或淋巴结外病灶;
l 应测量每个病灶的最长(LDi)和最短直径;
l 病灶应来自不同部位,并代表总体疾病负担;
l 病灶应包括任何纵隔或腹膜后疾病;
l 对于结节病灶,LDi应> 1.5 cm,对于结外病灶,LDi应> 1.0 cm;
应在CT横断面上测量每个病灶的最长直径和最短直径,然后将每个病灶的值相乘以得出每个病灶的“直径乘积”(PPD),再将它们加在一起得出“直径乘积之和”或SPD。该SPD将作为在FDG PET/CT中期和治疗结束时对CT上肿瘤负荷进行顺序量化的基线。病灶用于FDG PET/CT随访。所有其他病灶均作为不可测量疾病(例如,皮肤,胃肠道,骨骼,肝脏,肾脏,心包积液,腹水)。
脾脏:
正常(Normal):影像学检查未达到脾异常(增大)的标准或影像学检查中显示脾切除;
增大(Enlarged):影像学检查中脾大小增加程度达到符合异常的标准:上下径长度>130mm;
无法评估(NE):无法通过影像学检查(如,影像数据质量不佳或缺失)对脾进行评估。注意:对于缺少腹部 CT/MRI 冠状位的图像,测量脾脏上下径时以脾脏显示层数乘以层厚来确定,其结果可能存在 5mm 的误差。
肝脏:主观判断
正常(Normal):评估者根据影像学检查进行专业判断没有肝肿大,或者受试者影像资料显示肝切除。肝没有局灶性FDG 摄取;
增大(Enlarged):评估者根据影像学检查进行专业判断肝肿大;
无法评估(NE):无法通过影像学检查(如,影像数据质量不佳或缺失)对肝进行评估。
(2)FDG-PET 5PS评分
Lugano 2014推荐使用PET 5PS半定量评分进行淋巴瘤临床试验包括中期分析和治疗结束后评估。PET 5PS评分可作如下定义:
l 1分,所有病灶代谢的摄取值不超过背景组织摄取;
l 2分,最高摄取病灶SUVmax≤纵隔血池SUVmax;
l 3分,纵隔血池SUVmax<最高摄取病灶SUVmax≤肝脏血池SUVmax;
l 4分,肝脏血池SUVmax<最高摄取病灶SUVmax≤ 2倍肝脏血池SUVmax;
l 5分,最高摄取病灶SUVmax> 2倍肝脏血池SUVmax。
(3)Lugano2014淋巴瘤治疗效果评价标准


Lugano分期中单独列出了FDG-PET和CT的评估标准,因此常常有人误解只需要单独根据PET或CT影像给出评估结果,或者在遇有PET评估和CT评估结果不一致时不知所措。针对该情形,淋巴瘤相关评估标准的第一作者Bruce Cheson博士曾发布白皮书对如何综合FDG-PET和CT给出总体评估进行了阐述,有如下原则:
对于获取FDG-PET的时间点,FDG-PET评估优先级高于CT缓解。
对于仅获取CT的时间点,在之前的FDG-PET评估后,CT评估可能受到之前PET-CT评估的影响。
例如:PET评估结果符合CR,CT扫描评估结果符合PR。后面时间点CT扫描仍然显示PR。在后面这一时间点,即使没有PET,总体评估结果为CR,除非另一次PET评估证明或CT扫描结果恶化。
03. 研究结果-疗效评估相关
根据IRC使用的Lugano2014评估标准,在1b期,9例患者中有6例缓解(ORR:66.7%),5例(55.6%)获得CR。在2期第一阶段入组8例患者,7例患者的疗效可评估;ORR为85.7%(6/7),5例患者(71.4%)达到CR,超过了预定的第二阶段入组疗效边界。在2期所有28例2期患者中,16例获得缓解,ORR为57.1% (16/28),CR率为46.4%(13/28)。在意向治疗人群(n=37)中,22例患者(59.5%)达到客观缓解,其中18例(48.6%)CR(见下表)。10例患者接受过检查点抑制剂(ICI)(6例)或西达本胺(4例)治疗,信迪利单抗联合西达本胺治疗后,分别有6例(60.0%,6/10)和4例(40.0%,4/10)患者获得ORR和CR。

04. 总结
Lugano 2014结合代谢学(PET-CT)、解剖学(CT/MRI)和整体疗效评估,评估淋巴瘤的疗效并正确反应药效。需要注意的是,该标准在应用中可能会遇到挑战或摸棱两可的问题,因此在实际操作中可能需要根据具体情况进行定制化修订。
参考文献:
[1] Cheson BD, Fisher RI, Barrington SF, et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol. 2014;32(27):3059-3068. doi:10.1200/JCO.2013.54.8800.
[2]Ricard F, Cheson B, Barrington S et al. Application of the Lugano Classification for Initial Evaluation, Staging, and Response Assessment of Hodgkin and Non-Hodgkin Lymphoma: The PRoLoG Consensus Initiative (Part 1-Clinical). J Nucl Med. 2023 Jan;64(1):102-108.
[3] Gao, Y., He, H., Li, X. et al. Sintilimab (anti-PD-1 antibody) plus chidamide (histone deacetylase inhibitor) in relapsed or refractory extranodal natural killer T-cell lymphoma (SCENT): a phase Ib/II study. Sig Transduct Target Ther 9, 121 (2024). https://doi.org/10.1038/s41392-024-01825-0.
临影医药
有临医药全资子公司,是第三方独立医学影像CRO (Independent Review Committee, IRC),为创新药物临床研究提供第三方独立影像评估服务,确保试验结果的客观性和科学性,加速临床试验、注册审批的进程,助力新药上市。
冯巧敏 撰写 秦维伟 审核