



 有临
有临
 2023.06.30
2023.06.30
 2333
2333
TRK抑制剂是一类靶向治疗药物,主要用于治疗携带NTRK融合基因的肿瘤。近年来,TRK抑制剂在抗肿瘤领域取得了显著的成果,展现出了巨大的治疗潜力。然而,随着市场竞争的加剧,各大制药公司争相研发新型TRK抑制剂,希望在这一领域抢占高地。本文旨在探讨TRK抑制剂的竞争现状及未来可能的发展方向。
抗肿瘤思路的革命性转变——不区分肿瘤来源的疗法
大多数癌症治疗方法都是针对发生在特定器官或组织中的癌症,比如乳腺癌、肺癌、结直肠癌。而不区分肿瘤来源的疗法(tumor-agnostic therapy)则是指,不论肿瘤起源于哪种器官或组织,只要肿瘤具特定分子层面的改变(基因异常或特定分子特征),且某种药物可以靶向这种分子层面的改变,就可以接受该药物的治疗[1]。
在不区分肿瘤来源的疗法实施中,检测肿瘤的基因或其他分子特征可以帮助医生决定哪种治疗方法可能最适合某个肿瘤患者,而不考虑肿瘤发生部位或肿瘤组织在显微镜下的病理学表现。因此,分子检测成为治疗选择中的重要影响因素。在癌症治疗个体化或精准医学快速发展的大趋势中,分子检测所扮演的角色愈发重要。
2018年11月,医疗界和制药行业迎来了一款FDA新批准上市的抗癌药物Vitrakvi®(拉罗替尼,larotrectinib),这是一款不区分肿瘤来源、用于初始治疗的靶向药,用于成人和小儿具有NTRK基因融合的实体瘤治疗。它也成为继PD-1抑制剂Keytruda®(帕博利珠单抗,pembrolizumab)后,全球第2个上市的不区分肿瘤来源的疗法[1]。
TRK靶点的“钻石”属性
拉罗替尼上市后,TRK作为一个“钻石”靶点的代表,迅速引起制药行业的重点关注。TRK(tropomyosin-related kinase,原肌球蛋白相关激酶)蛋白是一类神经生长因子受体,属于酪氨酸激酶。TRK家族共包含3个高度同源的蛋白——TRKA、TRKB、TRKC,分别由NTRK1、NTRK2和NTRK3基因编码。TRK与细胞增殖、分化、代谢、凋亡等密切相关[2]。异常激活的TRK信号可影响肿瘤细胞的增殖和生存。TRK信号通路的改变主要包括NTRK基因融合、蛋白过表达、单核苷酸改变和剪接变异,其中NTRK基因融合是最明确的致癌驱动因素。TRK抑制剂通过阻断异常激活的TRK信号传导,抑制肿瘤细胞的生长、增殖、迁移和侵袭能力,从而发挥抗肿瘤的作用。
需要注意的是,并非所有NTRK基因的结构重排都会产生嵌合RNA和蛋白质,因此,患者是否携带NTRK融合基因、融合蛋白的类型和表达水平等,都可能影响到TRK抑制剂的疗效。在使用TRK抑制剂进行治疗之前,需要使用足够可靠的方法来对NTRK融合进行检测来确定患者是否适合接受该治疗。
然而,所谓“钻石”靶点,除了意味着针对该靶点的药物临床疗效十分显著外,也意味着它非常罕见。在中国常见的肺癌、乳腺癌、结直肠癌中,只有不足1%的患者存在NTRK融合。而一些发病率极低的瘤种中,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的概率却超过90%(见下图)。综合而言,每年新发肿瘤患者中,仅有约不到0.3%的患者存在NTRK融合。
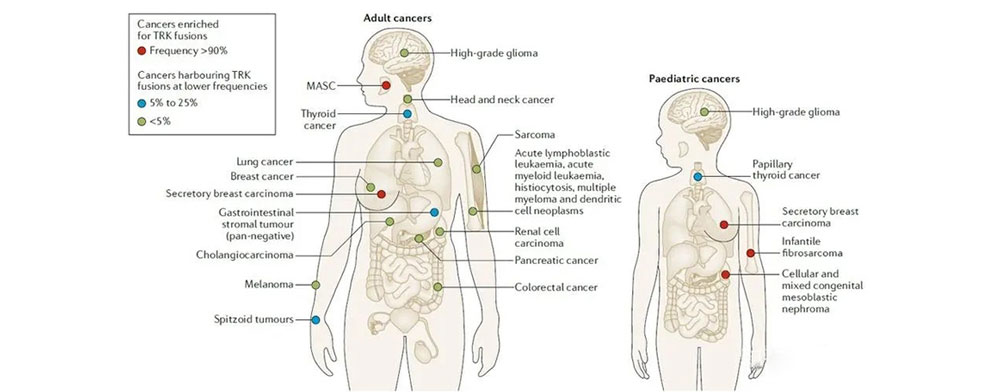
TRK抑制剂的当前竞争格局
目前,市场上已有2款TRK抑制剂获得批准上市,包括前述的拉罗替尼(Vitrakvi®)和后来的恩曲替尼(entrectinib,Rozlytrek®)。这两种药物在临床试验的NTRK融合阳性受试者中展现出了超过70%的客观有效率,并凭借II期研究数据获得上市批准,并迅速获得上市国家临床指南的标准治疗推荐。这两款药物的成功标志着个体化靶向治疗的突破,进一步验证了不区分肿瘤来源治疗策略的可行性,为肿瘤治疗带来了新的希望和机遇。
拉罗替尼和恩曲替尼的成功为其他制药公司开发TRK抑制剂赋予了巨大信心,随着越来越多的TRK抑制剂进入市场,竞争也日趋激烈。各大制药公司纷纷加大研发投入,以期开发出更具竞争力的产品。截至2023年3月,在中国NMPA登记、正在开展的临床试验就已多达19项(见下表),而正处于临床前阶段和正在申报临床的药物仍有20多个。可以预见,在未来几年内,TRK抑制剂的临床开发将会进入激烈的竞争阶段,正在进行和即将开展的临床试验将会争夺为总体上数量稀少的NTRK融合阳性肿瘤患者。
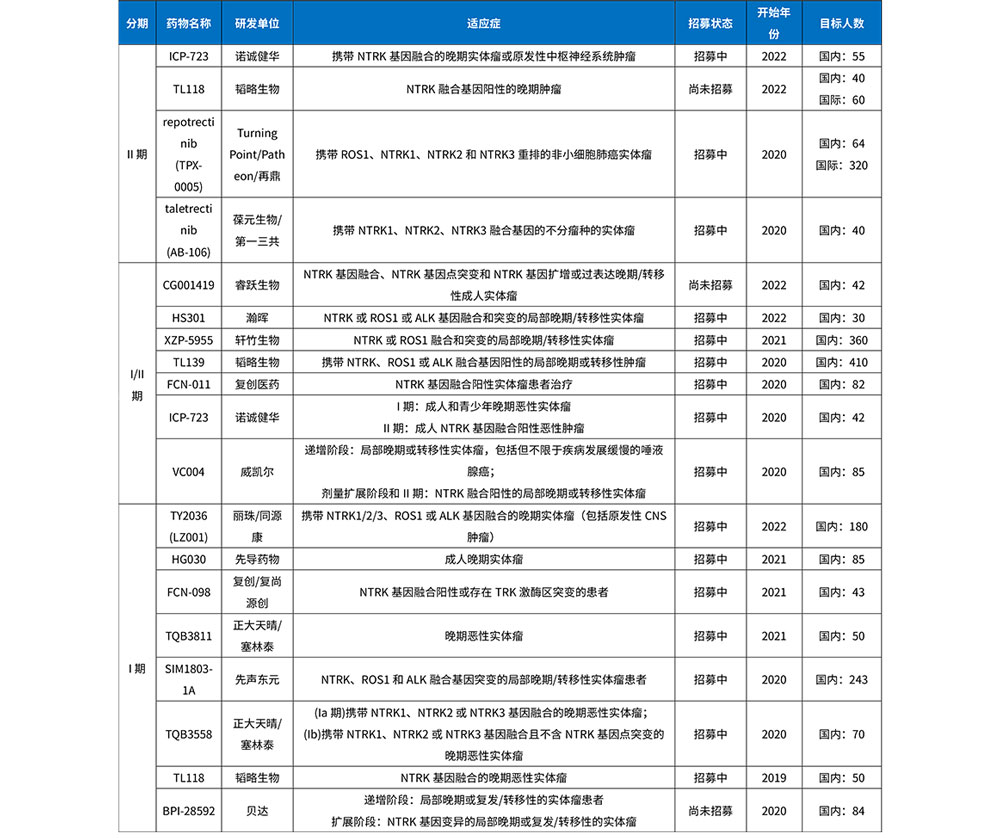
新的出路在何方?
TRK抑制剂治疗潜力巨大,但目标患者整体数量稀少,在这一背景下,如何在竞争激烈的市场中寻求新的出路,成为了各大制药公司面临的挑战。面对TRK抑制剂市场的竞争格局,笔者认为有以下几个方向值得关注:
● 针对耐药性研发新型TRK抑制剂
抗肿瘤治疗中,耐药性一直困扰着靶向治疗疗效的维持。尽管已经上市的第一代TRK抑制剂拉罗替尼和恩曲替尼有着超高的客观缓解率与缓解持续时间,但仍然面临肿瘤耐药的问题。目前的临床研究结果已经明确的耐药突变包括G595R、G623R、F589L、G667C等,一旦出现耐药突变,拉罗替尼和恩曲替尼的疗效均不理想。根据已知的耐药性机制,并继续研究其他潜在的耐药机制,研发相应的第二代、第三代TRK抑制剂,将有助于提高靶向治疗效果,为患者带来更好的生存质量。
● 积极推动罕见靶点分子诊断的落地普及
对于罕见的“钻石”靶点,分子检测结果符合药物特性是治疗选择中的先决条件。可能与NTRK发生融合的伙伴基因数量较多,一代TRK抑制剂耐药突变类型复杂,操作简单、易普及的IHC筛查可靠性有限。《中国实体瘤NTRK融合基因临床诊疗专家共识》指出:使用覆盖NTRK基因内含子区域的NGS DNA panel或者全外显子组检测作为NTRK融合基因检测的首要手段,NGS RNA panel或者转录组作为NTRK融合基因检测的重要补充手段[3]。NGS RNA panel比DNA panel具有更高的灵敏性,并行开展DNA和RNA测序,能够更精准地找到目标患者,为患者提供更优质的治疗方案。
制药工业界应积极推动研发更低成本、更易操作的核酸测序设备和耗材,并应联合医疗服务提供方将其作为新型基础设施在更广泛的地域落地,提高先进分子诊断技术的普及率,最终将惠及更多携带罕见驱动突变的肿瘤患者。
● 优化药物性能
Repotrectinib是新型TRK抑制剂,它在分子结构设计上具有更为紧凑的三维大环结构,使其能够精准铆合到ATP结合位点,有助于降低耐药突变带来的疗效下降,为第一代TRK抑制剂耐药后的再治疗提供新的选择。该药有望今年在我国和美国上市的。Repotrectinib作为新型TRK抑制剂的典型代表,显示了提高药物的选择性和结合能力、优化药物稳定性进行优化、降低药物毒性、减少耐药的发生率,将有助于提高TRK抑制剂的市场竞争力。
总之,TRK抑制剂市场竞争激烈,制药企业需要不断创新、研发新型药物,以期在竞争中占得先机。同时,关注分子诊断普及、药物性能优化等方向,将有助于寻找新的市场出路。
参考文献
[1] Looney, Ann-Marie et al. “Tumour-agnostic therapies.” Nature reviews. Drug discovery vol. 19,6 (2020): 383-384. doi:10.1038/d41573-020-00015-1
[2] Gambella, Alessandro et al. “NTRK Fusions in Central Nervous System Tumors: A Rare, but Worthy Target.” International journal of molecular sciences vol. 21,3 753. 23 Jan. 2020, doi:10.3390/ijms21030753
[3] Xu, Chunwei et al. “Expert consensus on the diagnosis and treatment of NTRK gene fusion solid tumors in China.” Thoracic cancer vol. 13,21 (2022): 3084-3097. doi:10.1111/1759-7714.14644
部分图片来源于网络