



 有临
有临
 2024.03.01
2024.03.01
 597
597

有临来雅(上海)数据科技有限公司成立于2019年,是上海有临医药的控股子公司,致力于给国内外创新药、疫苗与医疗器械企业提供临床试验统计咨询、试验设计和方案撰写、数据管理、统计分析与编程等多方面专业服务。团队由数十位来自国内外知名药企和临床CRO,拥有平均十年左右行业经验的核心技术人员及专家构成。
随着有临来雅不断追求卓越、深化专业领域的步伐,我们荣幸地宣布,有临来雅正式成为CDISC(临床数据交换标准协会)的企业会员,展现了我们对规范化、高效化、国际化临床研究数据标准的不懈追求。

张子豹博士
有临来雅总经理
曾任CDISC中国区(C3C)主席和CDISC亚太区(AP3C)主席,一直积极推广该全球标准,促进临床试验数据全流程规范和高效。张博士拥有逾20年的生物医药行业经验,包括技术团队管理、商务拓展、创业投资和企业管理。曾在多家跨国临床CRO公司负责中国区域的统计团队建立和管理;当前聚焦企业管理,致力于打造国际品牌并为客户提供高品质的临床CRO服务。张子豹拥有复旦大学博士学位,中欧国际工商学院Global EMBA学位以及创投课程学习经历。有临来雅统计分析与编程团队核心成员均有多年医药行业经验以及CDISC标准咨询、培训以及实施经验,已支持国内外多家药企CDISC标准为基础的电子数据递交(e-submission data package)。
作为临床研究数据领域的权威机构,CDISC为全球医药企业和研究机构提供了一整套统一的数据标准和管理规范,如下图显示。
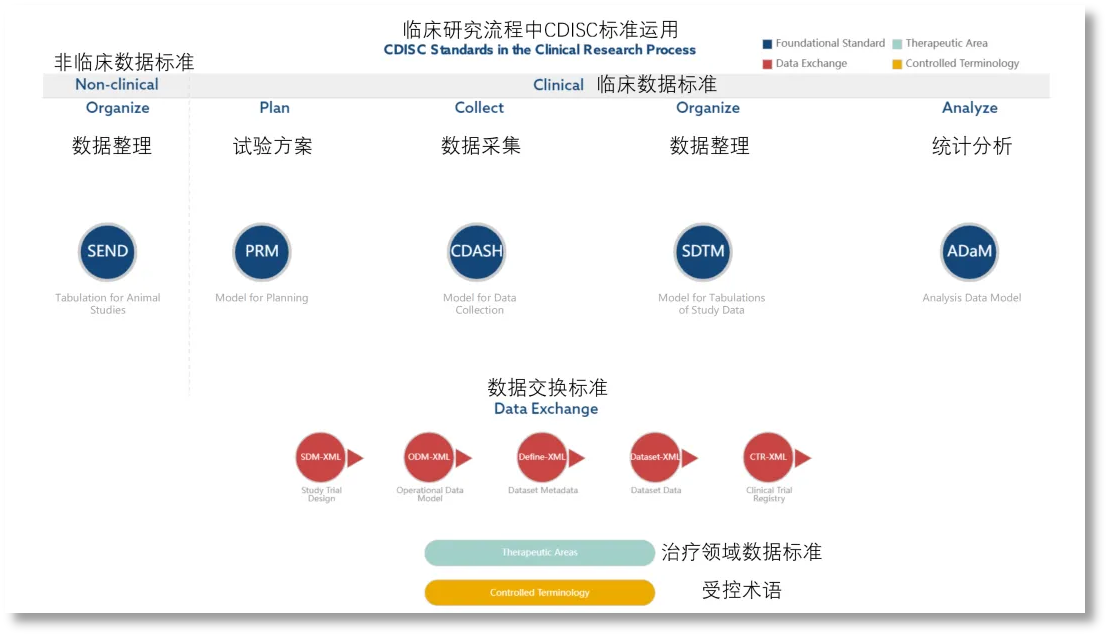
图 CDISC标准(https://www.cdisc.org/standards)
成为CDISC企业会员
意味着有临来雅将给我们的客户
带来以下一系列的益处
提升数据质量与一致性
通过遵循CDISC的标准,企业可以确保其在临床试验和其他研究过程中收集的数据具有更高的一致性和
准确性。这有助于减少数据错误、重复和冗余,提高数据的质量。
简化数据交换和集成
CDISC的标准促进了不同系统之间的数据交换和集成。这使得企业可以更容易地将数据从一个系统迁移到另一个系统,或将不同来源的数据整合在一起进行分析。
加速药物研发过程
通过使用CDISC的标准,企业可以简化临床试验数据的收集、管理和分析过程,从而加速药物的研发周期。这有助于企业更快地推出新药和治疗方法,满足市场需求。
降低合规风险
遵循CDISC的标准可以帮助企业满足监管机构的合规要求,降低因数据问题而导致的合规风险。
这对于需要在全球范围内开展业务的企业尤为重要。
促进数据共享和协作
CDISC的标准促进了不同组织之间的数据共享和协作。这使得企业可以更容易地与合作伙伴、监管机构和其他利益相关者共享数据,共同推动科学研究和医学进步。
在未来的日子里,我们将继续秉持“以客户为中心,以数据为驱动”的理念,不断提升临床研究数据的管理水平和服务质量,为我们的客户提供最优质的服务,最贴心的解决方案。选择有临来雅,就是选择了品质与创新的保障。我们期待与您携手共进,共筑临床研究数据的新未来!
有临来雅
上海有临医药子公司,成立于 2019 年,致力于给国内外创新药、疫苗与医疗器械企业。提供临床试验统计咨询、试验设计、数据管理统计分析与编程等多方面专业服务。团队由数十位来自国内外知名药企和临床 CRO,拥有平均十年左右行业经验的核心技术人员及专家构成。洞悉行业政策及标准,以客户需求为导向,不断优化迭代形成最佳实践和服务模式。适应不同业务需求,开创灵活创新的合作模式: 包括数统全方位大包服务、业务流程外包(FSP)、战略合作、专家咨询与培训、监督管理及人员外派。为客户降本增效,加速新药研发与上市进程。
统计分析与编程服务
有临来雅统计分析与编程团队致力于为客户提供卓越的一站式CDISC标准服务,包括将EDC系统收集的原始数据精准地转换成符合SDTM标准的数据集、生成ADaM数据集以及提供标准化数据电子递交包 (注释病例报告表、SDTM/ADaM define.XML、cSDRG和ADRG等),更好地支持临床试验注册和上市申请。有临来雅团队还可以提供其他CDISC标准实施,包括按CDASH标准设计CRF和EDC搭建、CDISC培训和策略咨询,以及基于CDISC标准的创新合作项目。
有临来雅