



 有临
有临
 2024.05.16
2024.05.16
 642
642
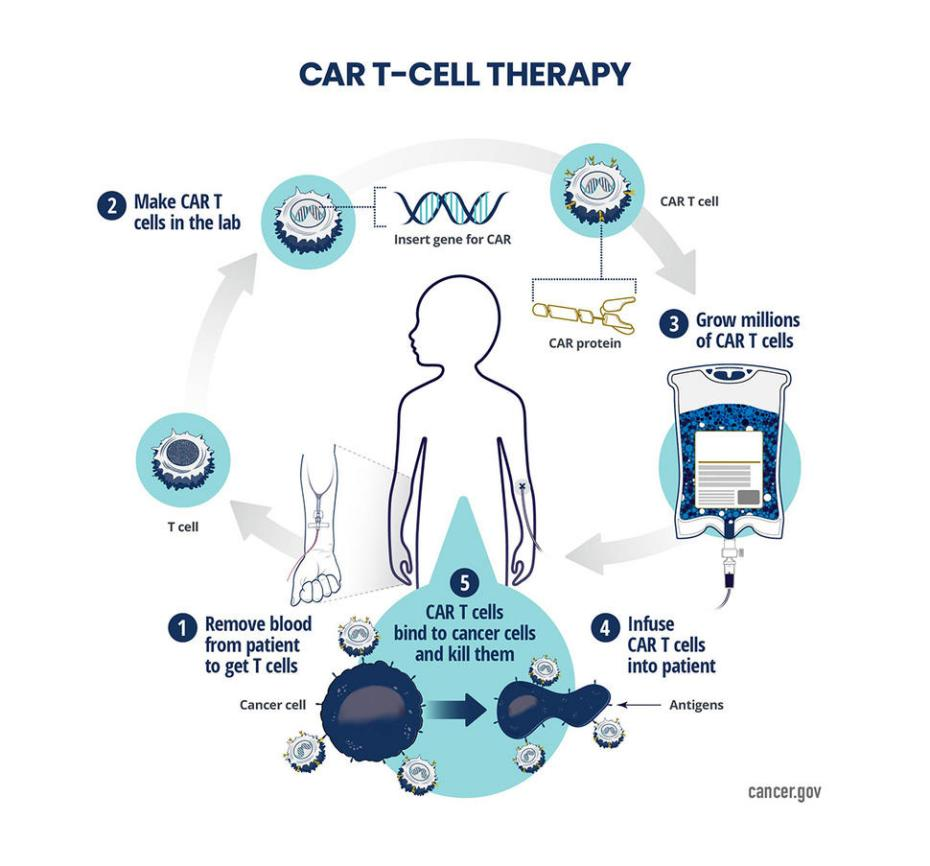
细胞治疗是一种前沿的生物医学技术,通过利用自体或供体的细胞,修复、替代或增强人体组织和器官功能,通过利用不同类型的细胞,实现对各种疾病的治疗,如白血病、心脏病和神经系统疾病等。细胞治疗按照细胞的种类可以分为干细胞治疗和免疫细胞治疗。免疫细胞是人体免疫系统的重要组成部分,主要包括T细胞、NK细胞和B细胞等。目前细胞治疗中相对成熟的就是CAR-T疗法。CAR-T细胞疗法是一种个体化的治疗策略,通过改造患者自身的T细胞,使其表达特定的嵌合抗原受体(CAR),以识别和攻击肿瘤细胞(如图1所示)。CAR-T细胞疗法作为一种创新性的免疫细胞治疗方法,随着CAR-T细胞疗法的不断发展,已经在临床治疗恶性肿瘤方面展示出了巨大的潜力。
CAR-T细胞的临床药理学评估包括药代动力学(暴露)、药效学(反应)和免疫原性研究。PK和PD研究为确定药品的安全性和有效性提供了重要信息。免疫原性研究评估对CAR-T细胞的免疫反应造成的潜在风险。CAR-T细胞临床药理学研究对于优化治疗方案、确保药物安全性和预测疗效至关重要。本文旨在探讨CAR-T细胞临床药理学研究的关键考量因素。
CAR-T细胞的药代动力学研究
与传统药物相比,CAR-T细胞由于“活体药物”的特性,输注后会在体内扩增并表现出独特的PK(也称为细胞动力学(CKs)),通常包括分布、扩增、收缩和持续四个不同的阶段(图2)。因此,常规药物的药代动力学研究如吸收、分布、代谢和消除(ADME)不能用于CAR-T的药代动力学研究,应按照规定的时间表收集样本,如血液和骨髓样本,以监测CAR-T细胞的体内持久性和增殖。对于系统暴露,应采集足够时间点的血液样本得出CAR-T细胞浓度-时间曲线。FDA推荐以下与CAR-T细胞扩增和持久性相关的PK测量:Cmax(峰浓度)、Tmax(达峰时间)、pAUC(曲线下局部面积);Clast(最后观察到的浓度);Clast时间;和t1/2(终末半衰期),其中t1/2应该谨慎解读,因为它们在很大程度上依赖于随访时间。部分暴露(pAUC)可用于暴露与疗效和/或安全性之间的相关性分析。为了评估可能影响CAR-T细胞体内扩增和持久性的因素,应同时考虑患者相关因素和产品相关因素,产品相关因素包括但不限于CAR-T细胞组成和分化状态。为描述CAR-T细胞在体内的动力学特征,FDA建议PK取样计划包括足够多的时间点,尤其是在扩增阶段,通常在输注后两周左右。可以通过测量转基因和CAR表达水平来监测CAR-T细胞的持久性。为了探索CAR-T细胞暴露与反应之间的关系,FDA建议尽可能对CAR-T细胞进行功能分析(免疫表型)和克隆性分析。
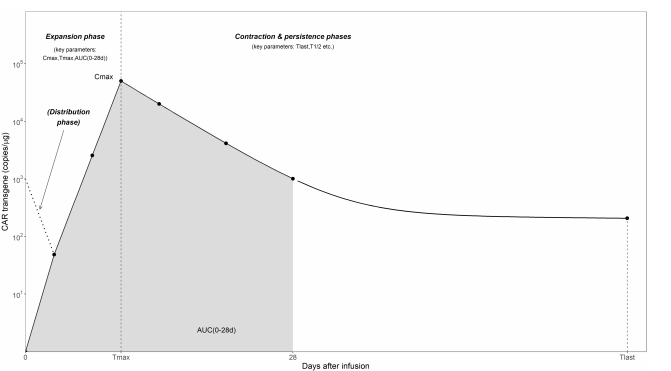
图2. CAR-T治疗的典型CK(浓度-时间)曲线,描述了其多相性质和关键CK参数。
CAR-T细胞疗法的药效学研究
CAR-T细胞疗法是通过识别和攻击肿瘤细胞来实现治疗效果。CAR-T细胞疗法可能引发免疫应答和治疗相关的毒性反应。药效动力学研究应重点关注CAR-T细胞疗法对机体免疫系统的影响,以及可能的免疫相关毒性反应。药效动力学研究对于评估CAR-T细胞疗法的治疗效果、确定最佳剂量和治疗方案以及预测疗效的持续时间至关重要。CAR-T细胞药效学评估包括细胞因子、趋化因子、免疫介质、肿瘤标志物(可溶性BCMA的血清水平和骨髓CD138+细胞)等水平变化,同时评价抗肿瘤活性,应答率等指标。
CAR-T细胞疗法的剂量-暴露-反应研究
目前CAR-T细胞疗法的疗效的暴露效应方面,与无应答患者相比,应答患者通常会有较高的扩增水平(Cmax和AUC0-28天),如在liso-cel治疗2L+LBCL(仅限非移植),以及ide-cel治疗多发性骨髓瘤中,更高扩增与更长的无进展生存期(PFS)相关。但不同适应症或研究之间也存在一定差异,可能是由于样本量较小。安全性的暴露-反应关系方面,CAR-T细胞活化和后续细胞因子释放导致的细胞因子释放综合征(CRS)是CAR-T细胞疗法主要的安全性事件。此外,神经系统事件(NE) 也是常见的安全性事件,但潜在的机制还未清楚。CAR-T细胞疗法中,对于CRS和NE,已经广泛评估了暴露-反应关系,通常情况下,不同CAR-T疗法中较高的扩增通常与较高的CRS和/或NE等级或发生率相关。细胞治疗的剂量-暴露-反应关系受到多种因素的影响,如受试者自身相关的因素如如受试者的疾病负荷、靶标表达和自身免疫状况,同时也受产品相关因素(如T细胞表型)的影响(图3)。
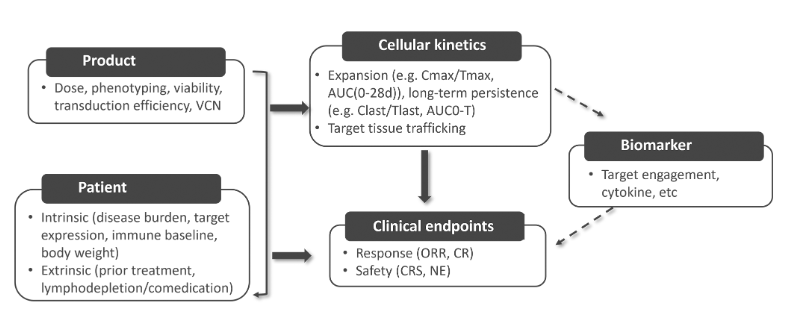
图3.可能影响细胞动力学和临床生物标志物或疗效和安全性终点的关键产品和患者相关特征的示意图。
CAR-T细胞疗法的免疫原性研究
细胞介导的免疫应答和ADA介导的补体激活,都有可能降低CAR-T细胞的扩增和持久性、影响安全性、或中和CAR结构域与肿瘤抗原结合的能力。FDA建议开发方法以检测产品开发过程中针对CAR-T细胞(CAR和共表达转基因,如适用)的体液和细胞免疫反应。可能影响CAR-T细胞免疫原性的患者相关因素和产品相关因素都应被考虑(图3)。需要注意的是,抗药物抗体(ADA)不太可能干扰基于qPCR的CAR-T药代动力学测定,但有可能干扰基于流式细胞术的CK。
CAR-T细胞疗法的临床药理研究是CAR-T细胞疗法发展和优化的关键领域。通过深入了解CAR-T细胞在体内的分布和代谢、与肿瘤细胞的相互作用、免疫应答和毒性反应,以及合理的临床试验设计和数据分析,可以更好地评估CAR-T细胞疗法的治疗效果、优化剂量选择和治疗方案,并预测疗效的持续时间和潜在的副作用。进一步的研究和探索在CAR-T细胞临床药效动力学研究领域是十分必要的,以不断改进CAR-T细胞疗法的临床应用,并为患者提供更有效的治疗策略。
参考文献:
1. Weber EW, Maus MV, Mackall CL. The Emerging Landscape of Immune Cell Therapies. Cell. 2020 Apr 2;181(1):46-62. doi: 10.1016/j.cell.2020.03.001. PMID: 32243795; PMCID: PMC8900215.
2. Considerations for the Development of Chimeric Antigen Receptor (CAR) T Cell Products, FDA, 2022.03.15.
3. Mody H, Ogasawara K, Zhu X, et al. Best Practices and Considerations for Clinical Pharmacology and Pharmacometric Aspects for Optimal Development of CAR-T and TCR-T Cell Therapies: An Industry Perspective. Clin Pharmacol Ther. 2023;114(3):530-557.
4. NIH http://cancer.gov.
5. Connarn, J.N. et al. Characterizing the exposure-response relationship of idecabtagene vicleucel in patients with relapsed/refractory multiple myeloma. CPT Pharmacometrics Syst. Pharmacol. https://doi.org/10.1002/psp4.12922 (2023).