



 有临
有临
 2024.09.06
2024.09.06
 1863
1863
111

根据前面两篇文章肿瘤试验疗效评估统计分析方法应用与实现的介绍我们了解到疗效指标根据数据类型大体分为两类:时间-事件指标(DOR、PFS和OS等)和二分类指标(ORR、DCR等),本文侧重于探讨如何解读时间-事件指标的统计分析结果。
01.时间-事件指标
肿瘤试验中时间-事件指标主要包括缓解持续时间(DOR)、无进展生存期(PFS)和总生存期(OS)等,属于生存随访资料,对该类资料进行的分析称作生存分析,生存分析的主要内容包括生存过程的描述、生存过程的比较和生存时间的影响因素分析等。生存过程的描述通常采用乘积极限法(product-limit method),更常见的名称是Kaplan-Meier法,简称KM法,早期临床试验中常常通过绘制KM曲线图探索研究药物的中位生存期,II、III期试验常常通过绘制不同治疗组别的KM曲线图直观比较组间疗效差异,生存过程的比较的检验方法有log-rank检验、Wilcoxon检验、似然比检验,生存过程的影响因素分析较为广泛的是Cox比例风险模型(Proportional hazards model),这里不对检验方法以及模型原理做详述,以解读统计分析结果为主。
1.1 生存概率和生存率的区别
生存分析中最基本的两个统计量就是生存概率(survival probability)和生存率(survival rate),两者虽然只有一字之差,但含义却相差甚远,生存概率指单位时间中开始存活的研究对象在结束时仍存活的比例,可用p表示,生存率指总的研究对象经过t个单位时间仍存活的比例,可用S(t)表示,若以年为单位时间,则生存概率可用以下公式表示:
![]()
若研究数据中无删失值,则生存率可用以下公式表示:
S(t) = t时刻仍存活的例数÷总研究例数
若研究数据中有删失值,则需要分时段计算不同单位时间的生存概率pi(i=1,2,...,t),然后根据概率乘法定理将pi相乘得到t时刻生存率,公式表示如下:
根据以上公式可以看出生存概率是针对单位时间而言的,生存率是针对某个时间段的(由单位时间组成的时间段),是生存概率的累计结果。临床试验中常用的5年生存率指的就是第1年存活、第2年仍存活...直至第5年仍存活的累计概率,而这5年间每年有不同的生存概率。
1.2 生存曲线和中位生存期
1.2.1 生存曲线
采用KM法绘制生存曲线图,横坐标为生存时间,纵坐标为生存率,将各个时间点的生存率连接在一起则为生存曲线,如下图 一,图中的每个o代表一个删失的受试者(不同项目中删失点的符号可能不一样,如用+表示,或者o,或其他,本文图例中删失符号为o),每一个阶梯代表发生了“事件”,随着时间的增加,生存曲线一般呈下降趋势,下降速度快在图形中表现为坡度大、曲线陡峭,意味着较低的生存率或较短的生存期;下降速度慢在图形中表现为坡度小、曲线平缓,意味着较高的生存率或较长的生存期。
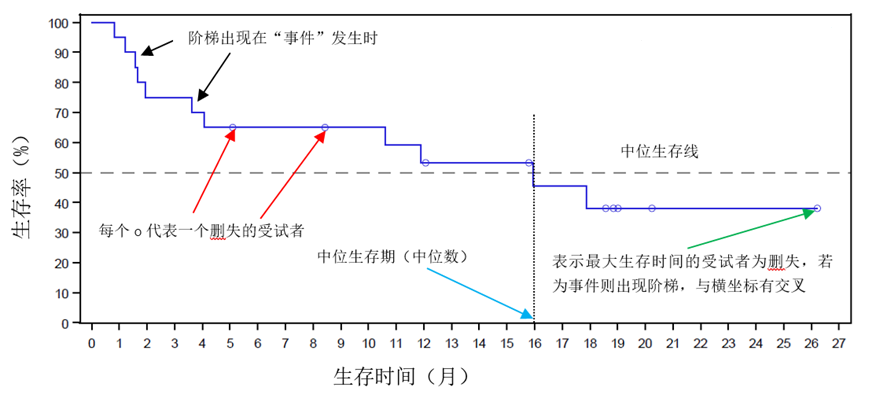
图一
以上生存曲线图是我们最常见的,即横坐标为生存时间,纵坐标为生存率,可简称为S图,若纵坐标为生存率的对数,则简称为LS图,若纵坐标为生存率对数的对数,则简称为LLS图,LS图和LLS图一般不作为结果展示,但是可以帮助我们选择分析结果。
1.2.1 中位生存期
另一个用来描述生存情况的统计量为中位生存期,也称半数生存期,即中位数,表示当且仅当50%个体尚存活的时间,见图一中横向虚线,虚线与KM图交叉点对应的横坐标值即为中位生存期,中位生存期越长,表示疾病预后越好,反之则预后越差。
注意:若研究数据中删失的例数非常多,可能会出现未达到中位生存期的情形,如下图二中的Disease Group 3,该情形的出现并不能说明样本中50%以上的受试者未发生事件,是否达到中位生存期与样本中50%的受试者是否发生了事件没有直接的关系。同样,中位生存期不能简单地理解为“死亡人数到了一半”或“存活人数还剩一半”,因为它有失访问题(即有删失情形),严格来说就是生存率为50%时所对应的时间t。
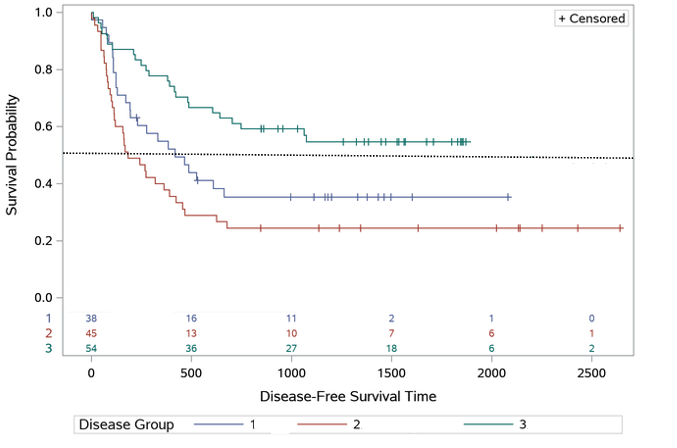
图二
1.3 生存曲线的比较
生存曲线的比较最简单直观的方法就是比较中位生存期大小,但是中位生存期有很多的局限性,比如受数据成熟度、随访时间、肿瘤免疫治疗特点等影响,可能导致无法计算、不够全面或不准确等,所以验证性试验中需要对生存分析做统计推断,即对总体生存曲线进行假设检验,以比较研究组和对照组间的疗效差异。
1.3.1 Log-Rank检验
常用的生存曲线比较方法为Log-Rank检验,它属于非参数方法,该方法并不指定生存时间服从某种特定的分布,所比较的是整个生存时间的分布,而不是仅仅比较某个特定时间点的生存率。假设检验如下,显著性水平α单侧常取0.025。
H0: S1(t) = S2(t),即两总体生存曲线相同
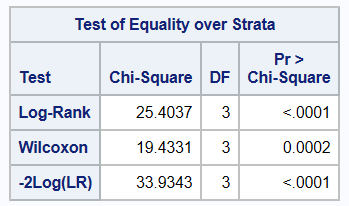
图三

以上图三中的Log-Rank检验结果(采用 SAS 9.4 软件的 proc lifetest过程)为例,卡方P值小于0.0001,拒绝H0,两生存区线组间差异有统计学意义,这时可通过中位生存期指标初步评价其差异程度。
Wilcoxon检验、似然比检验(-2Log(LR))和Log-Rank检验类似,通过检验的P值大小推断生存曲线间差异是否有统计学意义。
注意:若Wilcoxon检验、似然比检验(-2Log(LR))和Log-Rank检验结果不一致,甚至差别很大时,如何抉择呢?一般情况下若组间生存曲线图大致平行时,Log-Rank检验比较常用,结果更可靠一些,但是若生存曲线有交叉,尤其是交叉比较明显时,采用Wilcoxon检验结果更可靠一些,但是若LS图近乎直线时,采用似然比检验结果更可靠一些。也有学者认为Wilcoxon检验结果主要反映了生存曲线早期或近期的差异情况,Log-Rank检验结果主要反映生存曲线晚期或远期的差异情况。
除P值外,有时还需要计算风险比(HR)比较组间差异程度,HR可简单理解为暴露于某因素与不暴露于某因素的“死亡”风险比(这里的“死亡”泛指结局,比如针对PFS指标,结局为死亡或疾病进展)。可根据Log-Rank检验的U和V统计量估计HR值及其95% CI,计算公式这里不详细描述,可参见参考文献《Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC》https://www.nejm.org/doi/full/10.1056/NEJMoa1913662中附件说明,截图如下:

图四
针对HR值(研究组相对对照组),通常若HR=1,则表示两组的疗效相同,若HR>1表示研究组劣于对照组,若HR<1表示研究组优于对照组,但在验证性试验中,更保守的评估不仅仅关注HR值,还需关注其95% CI,通过比较置信区间的上限或下限与1的大小关系判断研究组是否优效或非劣效,可参考以下图五。
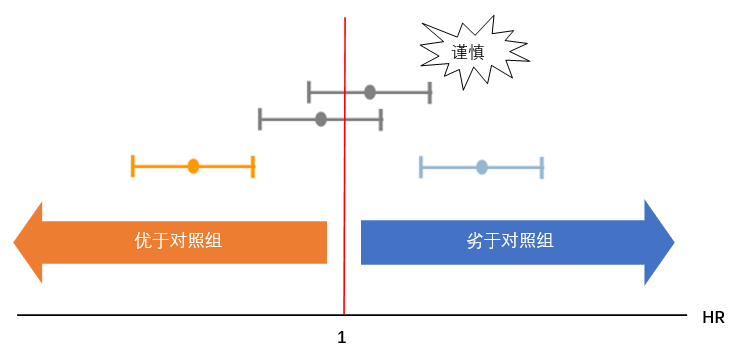
图五
1.3.2 Cox比例风险模型
以上介绍的Log-Rank检验属于生存曲线比较的单因素分析方法,若生存曲线有交叉,则可能提示存在某种混杂因素,或研究者关心的影响生存率的因素不止一个、或者出于探索目的,需要考察多因素对生存率的影响,则采用分层的办法或多因素的办法来校正混杂因素,例如构建多因素的Cox比例风险模型。因此,也可采用Cox比例风险模型中的风险比(HR)比较组间差异程度。
注意:该模型的重要前提假设是等比例风险,它表示某因素对生存的影响在任何时间都是相同的,不随时间的变化而变化,如某基因对肿瘤的影响,不管是第一年、第二年、... ,对肿瘤的危险都是相同的,只有满足这一条件,才能应用Cox比例风险模型。
如果发现或怀疑某因素不满足等比例风险假设,需要采取一定的补救措施,通常若该因素为非主要研究因素,可以将其分层校正,若是主要研究因素,需加入该研究因素与时间的交互项。
1.3.3 简单示例
我们以2024年6月3日上海交通大学附属胸科医院的陆舜教授在《新英格兰医学杂志》发表题为“Osimertinib after Chemoradiotherapy in Stage III EGFR-Mutated NSCLC”的主要研究终点PFS统计分析结果为例(图六),Osimertinib组的PFS中位生存期为39.1个月,Placebo组的PFS中位生存期为5.6个月,Osimertinib组的KM曲线约从3个月开始一直高于Placebo组,无交叉,PFS曲线差异性检验的P值小于0.001,HR值为0.16,95% CI为0.10-0.24,其上限(0.24)远小于1,结果表明:Osimertinib可显著延长
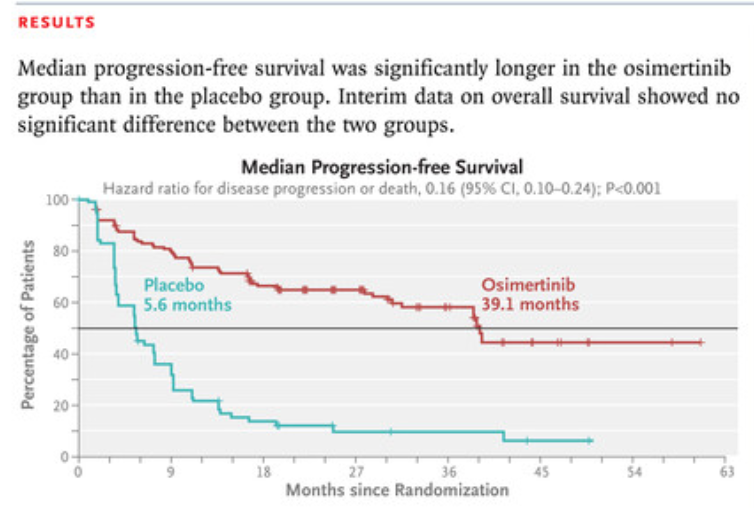
图六 EGFR 突变 Ⅲ 期不可切 NSCLC 患者的PFS。
参考文献:
1.《医学案例统计分析与SAS应用》第1版,北京大写医学出版社。
2.《医学统计学》第2版,人民卫生出版社。
3.《Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC》,https://www.nejm.org/doi/full/10.1056/NEJMoa1913662。
4.《Osimertinib after Chemoradiotherapy in Stage III EGFR-Mutated NSCLC》,https://www.nejm.org/doi/full/10.1056/NEJMoa2402614。
李纪杰 撰写,冯雪、王素丽、章飞燕及张子豹 审核